
Suatu larutan cuka makan mengandung 6 asam asetat. Ji...
Kelarutan atau solubilitas adalah kemampuan suatu zat kimia tertentu, zat terlarut ( solute ), untuk larut dalam suatu pelarut ( solvent) [1] Kelarutan dinyatakan dalam jumlah maksimum zat terlarut yang larut dalam suatu pelarut pada kesetimbangan. Larutan hasil disebut larutan jenuh.

Dalam 250 mL larutan terdapat 17,1 gram zat non elektroli...
Suatu larutan terdiri atas dari dua komponen yang penting. Biasanya salah satu komponen yang mengandung jumlah zat yang lebih banyak disebut pelarut (solvent). Pelarut dipandang sebagai pembawa atau medium zat terlarut yang dapat berperan serta dalam reaksi kimia. Kemudian, komponen lainnya yang mengandung zat yang lebih sedikit disebut zat.

Cara Menghitung Ph Larutan Asam Kuat Dan Asam Lemah Panduan Kimia Riset Sexiz Pix
Larutan adalah campuran homogen yang terdiri dari dua zat atau lebih. Pelajari pengertian larutan & sifat sifat larutan di artikel ini!. Komponen-komponen suatu campuran gak bisa dipisahkan menggunakan filtrasi atau saringan (karena udah homogen). Baca juga: Mengenal Larutan Alkohol dan Fungsinya - Materi Kimia Kelas 12.
PEMBUATAN LARUTAN 1000 ML Na2S2O3 0,1 N DARI PADATAN Na2S2O3 5H2O
Jadi, jika dalam suatu larutan terkandung Pb(NO3)2 0,05 M dan HCl 0,05 M, maka akan terjadi endapan PbCl2. Itulah pembahasan tentang kelarutan dan hasil kali kelarutan. Untuk meningkatkan pemahaman tentang materi ini, Quipperian bisa sering-sering mengerjakan latihan soal ya. Jika bingung mendapatkan latihan soalnya, silahkan gabung bersama.
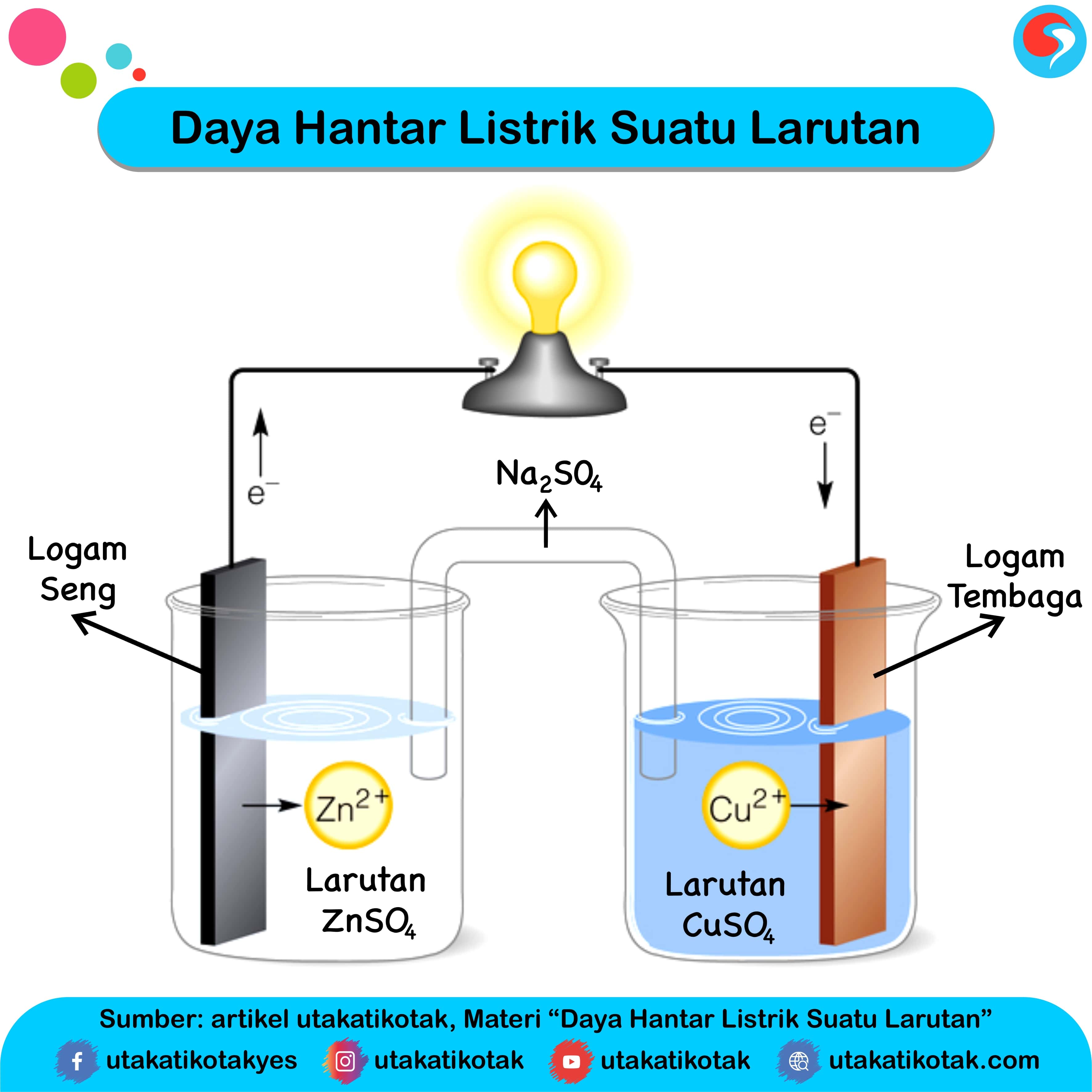
Daya Hantar Listrik Suatu Larutan
Mengutip e-modul Kimia: Peranan Elektrolit dalam Tubuh (2017) yang diterbitkan Kemdikbud, definisi larutan adalah campuran homogen yang tersusun dari pelarut dan zat terlarut. Secara umum larutan kerap dikenal dalam bentuk zat cair. Namun, sebenarnya larutan juga bisa berbentuk gas dan padat. Contoh larutan berupa gas adalah gas nitrogen.

Suatu Larutan Yang Dibuat Dengan Melarutkan 1 Mol Na2so4
Pengertian Konsentrasi Larutan. Konsentrasi larutan adalah besaran yang menunjukkan kepekatan suatu larutan melalui perbandingan antara pelarut dan zat terlarut. Jika zat terlarutnya banyak, maka larutan yang dibentuk memiliki konsentrasi tinggi (pekat). Sebaliknya, jika zat terlarutnya sedikit, larutan yang dibentuk memiliki konsentrasi rendah.
PPT LARUTAN ASAM, BASA DAN GARAM PowerPoint Presentation, free download ID6199614
Jadi, volume larutan setelah pengenceran adalah 1.000 mL, berarti volume pelarut yang ditambahkan: ∆V = V 2 - V 1 = 1.000 - 100 = 900 mL. Contoh 4. Larutan HCl 0,1 M sebanyak 100 mL dicampurkan dengan 150 mL larutan HCl 0,2 M. Tentukanlah konsentrasi larutan setelah dicampurkan! Pembahasan: Ingat, rumus molaritas pencampuran adalah:

Konsentrasi Larutan dan Pengenceran Larutan adalah suatu zat
Faktor-faktor ini secara tepat dijelaskan oleh hukum Lambert dan Beer. Hukum Beer-Lambert menyatakan bahwa energi yang diserap atau ditransmisikan oleh suatu larutan berbanding lurus dengan absorptivitas molar larutan dan konsentrasi zat terlarut. Hukum ini banyak digunakan dalam kimia analitik untuk mengukur absorbansi berbagai sampel.

Soal Larutan Asam dan Basa 2021 Bagian1 Urip dot Info
Istilah "pH" berasal dari kata Jerman "potenz," yang berarti "pangkat" , dikombinasikan dengan H, simbol unsur untuk hidrogen, jadi pH adalah singkatan dari "pangkat hidrogen.". Pengertian pada umumnya, pH (Power of Hydrogen) adalah skala yang digunakan untuk menyatakan tingkat keasaman atau kebasaan yang dimiliki oleh suatu larutan.. Skala dari pH terdiri dari angka 1 hingga

fraksi mol natrium hidroksida(Mr 40)suatu larutan
Tanpa Sobat pintar sadar, Sobat Pintar sudah membuat suatu larutan nih dalam ilmu kimia. Foto oleh Artem Podrez dari Pexels. Apa yang dimaksud Larutan ? Pengertian larutan adalah campuran homogen dari dua atau lebih zat. Nah, larutan terdiri dari zat terlarut dan zat pelarut yang sifatnya homogen. - Zat pelarut: zat yang melarutkan zat lainnya.

SifatSifat Larutan Asam, Basa dan Garam
Suatu larutan termasuk ke dalam larutan jenuh ketika terjadi kesetimbangan antara zat terlarut dan zat pelarut. Pada larutan jenuh partikel-partikelnya tepat bereaksi dengan pereaksi atau mengalami konsentrasi maksimal. Baca juga: Bulu Tangkis: Sejarah, Aturan Permainan, dan Teknik Dasarnya.

Suatu larutan mengandung garam Pb(NO3)2, Mn(NO3)2, dan Zn...
D. Suatu larutan sebanyak 1 L harus mengandung 360 g NaCl agar NaCl dapat larut. E. Suatu larutan sebanyak 1 L hanya dapat melarutkan paling banyak 360 g NaCI. Jawaban: E. Suatu larutan sebanyak 1 L hanya dapat melarutkan paling banyak 360 g NaCI. Pembahasan: Kelarutan merupakan jumlah maksimum suatu zat yang dapat larut dalam suatu larutan.
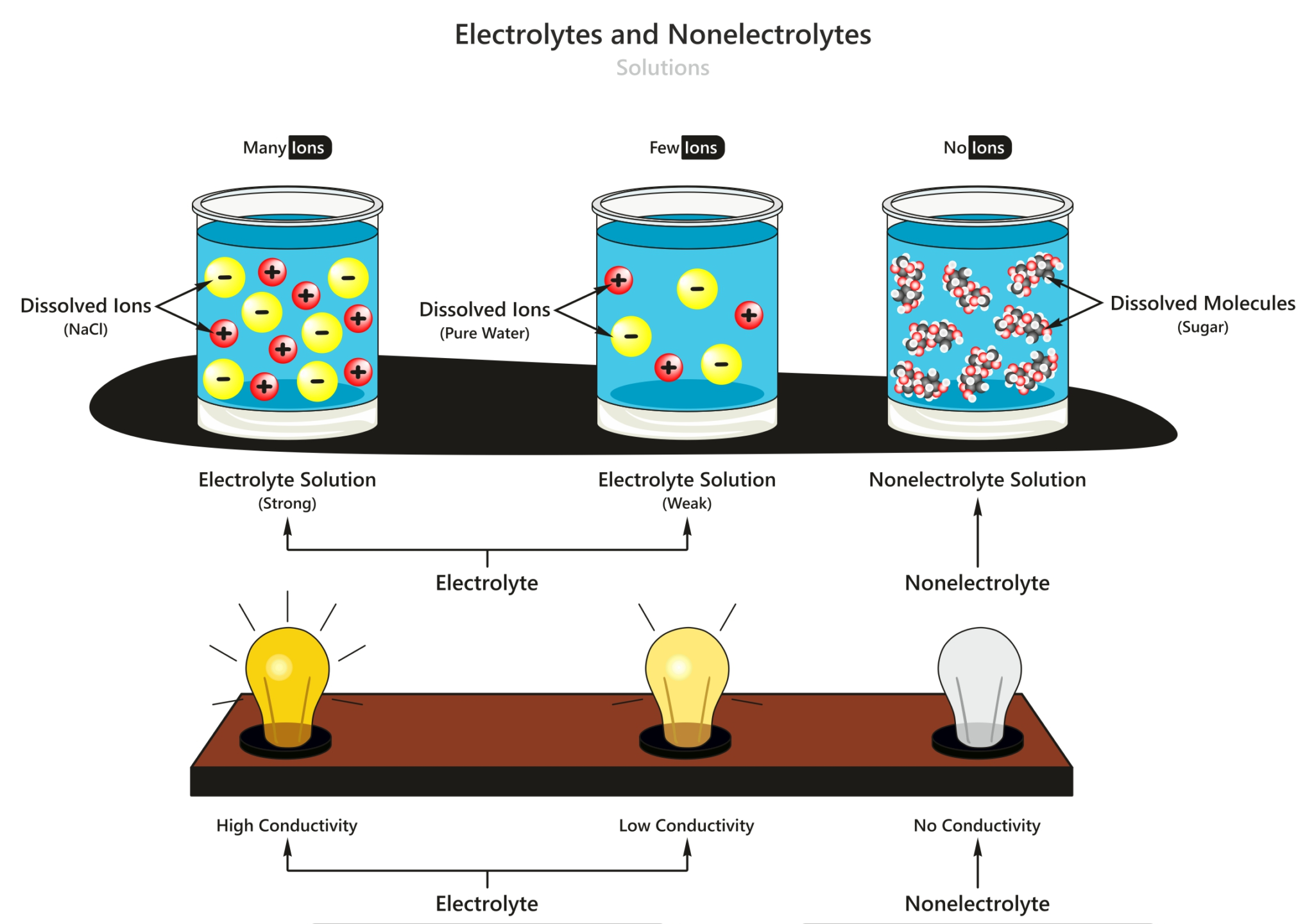
Larutan Elektrolit dan Non Elektrolit Materi Kimia Kelas 10
Larutan ideal. Diagram tekanan uap (p, x) pada campuran benzena/toluena pada suhu 20°C. Bila interaksi antarmolekul komponen-komponen larutan sama besar dengan interaksi antarmolekul komponen-komponen tersebut pada keadaan murni, terbentuklah suatu idealisasi yang disebut larutan ideal. Larutan ideal mematuhi hukum Raoult, yaitu bahwa tekanan.

Suatu larutan gula (Mr = 342 g mol^1) membeku pada suhu
Konsentrasi Larutan. Dalam ilmu kimia, konsentrasi adalah ukuran yang menggambarkan banyaknya zat di dalam suatu campuran dibagi dengan volume total campuran tersebut. Terdapat empat macam deskripsi kuantitatif konsentrasi, yaitu konsentrasi massa, konsentrasi molar, konsentrasi jumlah, dan konsentrasi volume.

Cara Menghitung Konsentrasi Larutan Dalam Persen
Jika suatu larutan bersifat asam, maka ia akan memerahkan lakmus biru. Sementara itu, jika larutannya bersifat basa maka ia akan membirukan lakmus merah. Jangan terbalik, ya! Terakhir, larutan atau senyawa asam bersifat korosif, sedangkan basa bersifat kaustik. Baca juga: Pengertian Isomer, Jenis-jenisnya, Serta Contohnya . Cara Membedakan Asam.

Suatu larutan dibuat dengan mencampurkan 100 ml larutan...
Sederhanya, suatu larutan terbentuk dari 10 bagian fruktosa yang terlarut dalam 90 bagian air. Misalnya, massa larutan adalah 100 gram, maka berat fruktosa adalah 10 gram dan berat air adalah 90 gram. Setelah mengetahui massa pelarutnya, kita dapat menghitung molalitasnya. Sehingga, molalitas larutan fruktosa 10% adalah 0,62 molal.