
Latihan Soal Dan Pembahasan Hasil Kali Kelarutan Dan Ion Senama.doc Pendidik Siswa
Definisi. Kelarutan (solubility) adalah jumlah maksimum suatu zat yang dapat larut dalam suatu pelarut. Satuan kelarutan umumnya dinyatakan dalam gram/L atau mol/L (M). Hasil kali kelarutan ( Ksp) dinyatakan sebagai hasil kali ion-ion (satuan Molar) dalam larutan jenuhnya, dengan masing-masing konsentrasi dipangkatkan koefisiennya.

Kumpulan Contoh Soal Kelarutan dan Hasil Kali Kelarutan Kimia Kelas 10 CoLearn
Contoh Soal Kelarutan dan Hasil Kali Kelarutan (KSP) dan Pembahasan Contoh Soal 1: Hitunglah kelarutan Cu(OH) 2 dalam satuan g/L, jika diketahui K sp Cu(OH) 2 = 2,2 × 10 −20. Pembahasan: Contoh Soal 2: Hitunglah kelarutan molar PbI 2 dalam larutan KI 0,1 M. (K sp PbI 2 = 7,1 × 10 −9) Pembahasan: Dalam larutan, KI akan terdisosiasi menjadi.

Contoh Soal Kelarutan Dan Hasil Kali Kelarutan Dan Pembahasannya Terbaru
Contoh Soal Kelarutan dan Hasil Kali Kelarutan. Suatu senyawa AB memiliki hasil kali kelarutan (Ksp) sebesar 2 × 1 0 − 6 2 \times 10^{-6} pada suhu tertentu. Jika kita memiliki larutan yang mengandung (A) dan (B).

Kelarutan dan Hasil Kali Kelarutan (Ksp) Kimia Kelas 11 • Part 5 Reaksi Pengendapan YouTube
Contoh Soal; Tetapan hasil kali kelarutan Kalsium Florida adalah 3,9 x 10-11.Tentukan konsentrasi ion kalsium dan florida pada larutan jenuh CaF 2 pada 25 o C, serta tentukan kelarutan garam tersebut dalam gram per liter.. Emulsi perak klorida untuk film fotografi dibuat dengan menambahkan garam klorida ke dalam larutan perak nitrat.

Kelarutan dan Hasil Kali Kelarutan (Ksp) Kimia Kelas 11 • Part 7 Contoh Soal Reaksi Pengendapan
Rangkuman 14 Kelarutan dan Hasil Kali Kelarutan. Rangkuman 15 Kelarutan dan Hasil Kali Kelarutan. Rangkuman 16 Kelarutan dan Hasil Kali Kelarutan. Rangkuman 17 Kelarutan dan Hasil Kali Kelarutan. Rangkuman 18 Kelarutan dan Hasil Kali Kelarutan. Kuis Akhir Kelarutan dan Hasil Kali Kelarutan. 675. 300. Materi pelajaran Kimia untuk SMA Kelas 11.

Soal Dan Pembahasan Kelarutan Dan Hasil Kali Kelarutan
Berikut ini beberapa garam dan K sp nya : 1) NiCO 3 , K sp = 1,4 x 10 -7. 2) MnCO 3 ,K sp = 2,2 x 10 -13. 3) CdCO 3, K sp = 6,2 x 10 -12. 4) CaCO 3, K sp = 8 x 10 -9. Urutan kelarutan senyawa tersebut dari terkecil ke besar adalah urutan 2,3,4,1. Whatsapp Twitter LinkedIn. Hasil Kali Kelarutan, Kelarutan, Kelarutan dan Hasil Kali Kelarutan.

Soal Kimia Bab Kelarutan Dan Hasil Kali Kelarutan Kelas 11 Binca Books
Simak Juga : Soal KSP (Kelarutan dan Hasil Kali Kelarutan) dan Pembahasan A. Kelarutan (Solubility) Istilah kelarutan (solubility) digunakan untuk menyatakan jumlah maksimal zat yang dapat larut dalam sejumlah tertentu pelarut.Kelarutan dinyatakan dalam mol/liter. Jadi, kelarutan sama dengan kemolaran dalam larutan jenuhnya. Contohnya, .kelarutan AgCl dalam air sebesar 1 x 10-5 mol L-1

Latihan Soal Kelarutan Dan Hasil Kali Kelarutan PDF
Latihan Soal Konsep Kelarutan & Hasil Kali Kelarutan (Sedang) Pertanyaan ke 1 dari 5. 1. Pertanyaan. Berikut ini reaksi ionisasi garam AB2 dalam air. AB2 ⇄ A2 + + 2B − Ksp = 1, 6 × 109. Perhatikan pernyataan berikut: Kelarutan garam AB2 dalam larutan A (OH)2 0,01 M adalah 4 × 10 − 8.

Kelarutan dan Hasil Kali Kelarutan (Ksp) Kimia Kelas 11 • Part 2 Soal Hubungan Kelarutan dan
Soal dan Pembahasan Kelarutan dan Hasil Kali Kelarutan No. 1 Diketahui kelarutan PbSO4dalam air pada suhu tertentu adalah 1,4 × 10−4 mol/L. Tentukan massa PbSO4 yang dapat larut dalam 500 mL air, nyatakan jawaban dalam satuan milligram (mg). (Ar Pb = 206; S = 32; O = 14) Pembahasan Diketahui: V = 500 mL = 0,5 L s.

Kelarutan (s) dan Hasil Kali Kelarutan (Ksp) Soal dan Pembahasan KIMIA KELAS 11 YouTube
1. Konsep & Hasil Kali Kelarutan. Di dalam materi ini, kamu akan mengenal konsep kelarutan & hasil kali kelarutan yang digunakan dalam ilmu kimia. Seperti yang sudah dijelaskan sebelumnya, kelarutan adalah jumlah maksimum suatu zat untuk larut di dalam sebuah larutan, sedangkan hasil kali kelarutan adalah hasil kali konstanta kesetimbangan pelarutan garam yang sukar larut dengan konsentrasi.
Soal Kelas 11 Kimia, Kelarutan dan Hasil Kali Kelarutan I Soal Sekolah
Untuk meningkatkan pemahaman Quipperian tentang materi kelarutan dan hasil kali kelarutan, simak contoh soal berikut. Contoh soal 2. Kelarutan Ag 2 CrO 4 dalam air adalah 10-4 M. Tentukan kelarutan Ag 2 CrO 4 dalam larutan K 2 CrO 4 0,01 M! Pembahasan: Reaksi kesetimbangan larutan Ag 2 CrO 4 adalah sebagai berikut. Dengan demikian, diperoleh:

TM 12 Kelarutan Dan Hasil Kali Kelarutan PDF
Video pembahasan soal kelarutan (s) dan hasil kali kelarutan (Ksp), dengan tahapan demi tahapan.Materi Kimia Kelas 11 SMA.#kelarutan #hasilkalikelarutan

Belajar Kelarutan Dan Hasil Kali Kelaruatan Dan Contoh Soal Kumpulan Contoh Soal
Soal No.19. Pada 25 o C, nilai Ksp Mg (OH) 2 adalah 3,2 x 10 -11. Hitunglah kelarutan Mg (OH) 2 di dalam larutan yang mempunyai pH = 12. PEMBAHASAN : Soal No.20. Kelarutan L (OH) 2 pada suhu tertentu adalah 2 x 10 -5 mol/L. Hitunglah kelarutan zat tersebut didalam 500 mL larutan yang mempunyai pH = 4 - log 2.

Contoh Soal Dan Pembahasan Tentang Kelarutan Dan Hasil Kali Kelarutan LEMBAR EDU
Video ini berisi penjelasan dan animasi tentang kelarutan dan hasil kali kelarutan (Ksp) yang dilengkapi dengan contoh-contoh soal.Video terkait :Pengaruh pe.

Contoh Soal Dan Pembahasan Tentang Kelarutan Dan Hasil Kali Kelarutan LEMBAR EDU
Berikut kami sajikan 10 contoh soal kelarutan dan hasil kali kelarutan beserta jawabannya. Pelajari dengan senang yah.. Jangan dibuat sulit. Contoh Soal Kelarutan dan Hasil Kali Kelarutan No.1-5 Soal No. 1 Diketahui Ksp Ag2CrO4 = 3,2 . 1011. Hitunglah kelarutan Ag2CrO4 dalam air.
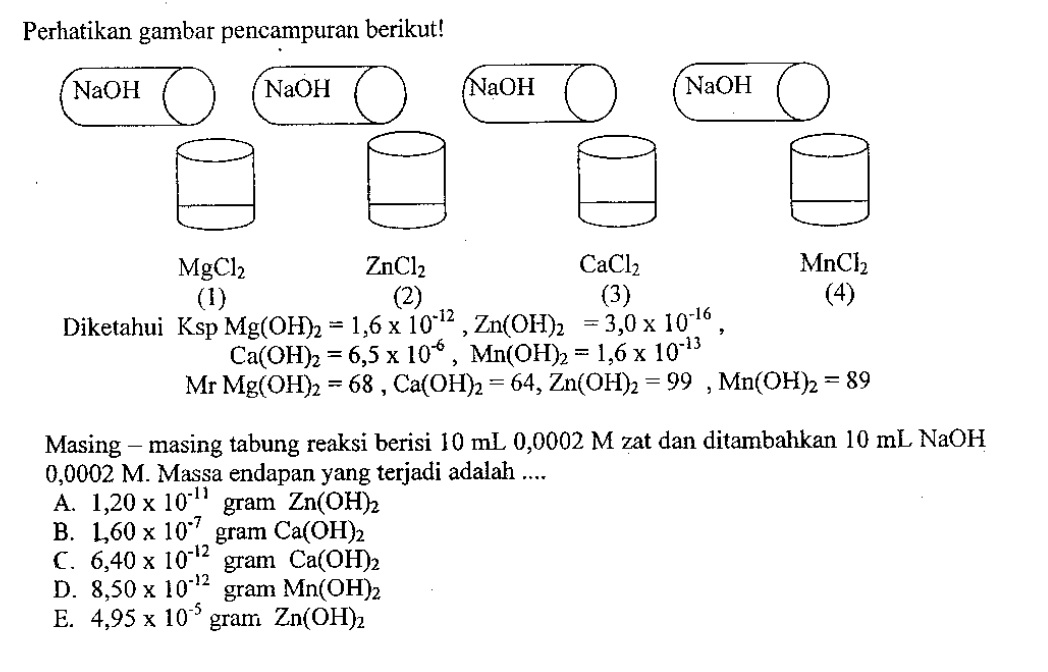
Soal Kelas 11 Kimia, Kelarutan dan Hasil Kali Kelarutan I Soal Sekolah
31 - 45 Soal KSP (Hasil Kali Kelarutan) Pilihan Ganda dan Jawaban. 31. Dalam 1000 mL larutan terdapat campuran garam- garam Ba (NO 3) 2, Sr (NO 3) 2, dan Pb (NO 3) 2 yang masing - masing konsentrasinya 0,01 M. Jika ditambahkan 81 miligram Na 2 CrO 4 (Mr Na 2 CrO 4 = 162) maka pada suhu 25°C, garam yang mengendap adalah . . .