
Cara Menghitung Jumlah Atom Dalam Suatu Senyawa Hal Images
Pembahasan Untuk menentukan jumlah atom yang menyusun suatu senyawa, maka terlebih dahulu harus mengetahui beberapa hal berikut ini: Angka kecil setelah lambang unsur (indeks), menyatakan jumlah dari atom yang dituliskan setelah lambang atom tersebut. Contoh: H2 maka jumlah atom H tersebut adalah 2.

Cara Mencari Rumus Molekul Unsur dan Senyawa Kimia Kelas 10 Belajar Gratis di Rumah Kapan
Rumus empiris dari suatu senyawa menunjukkan jumlah atom relatif dari masing-masing unsur dalam molekul senyawa tersebut dengan rasio (perbandingan) bilangan bulat paling sederhana. Sebagai contoh, rumus empiris dari asam askorbat adalah C 3 H 4 O 3, di mana perbandingan jumlah atom karbon, hidrogen, dan oksigen adalah 3 : 4 : 3.
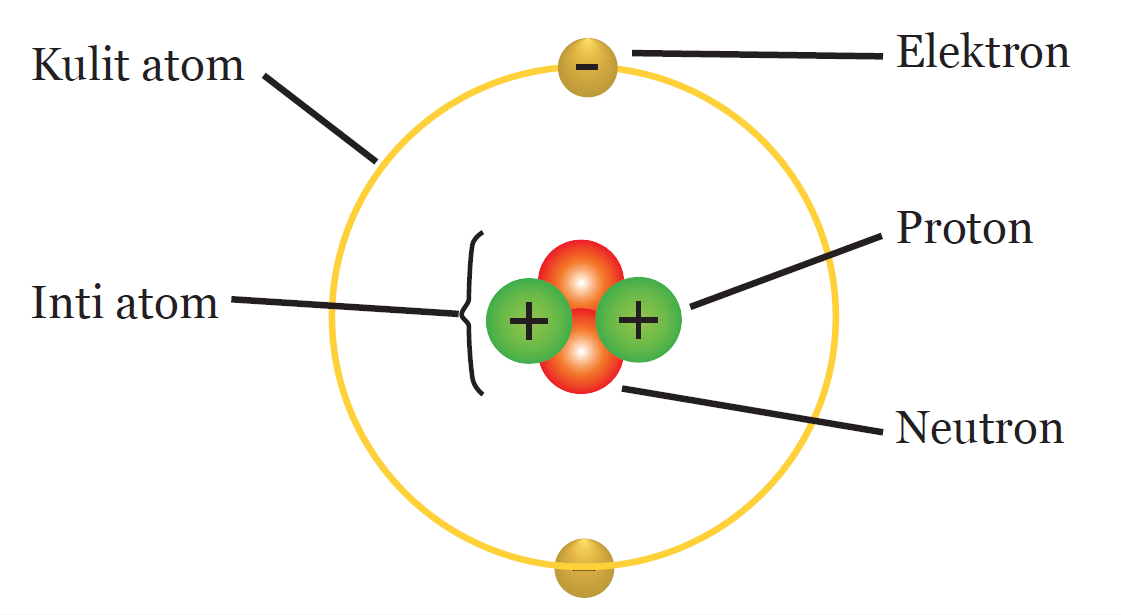
3 Partikel Penyusun Atom Materi Kimia
Untuk menghitung jumlah elektron yang tersisa, Anda mengurangkan jumlah muatan dari nomor atomnya. Dalam kasus ion positif, jumlah proton lebih banyak daripada elektron. Misalnya, Ca 2+ memiliki muatan +2 sehingga ion kehilangan 2 elektron dari keadaan netralnya. Nomor atom kalsium adalah 20.

Cara Menghitung Jumlah Atom Dalam Rumus Kimia Menghitung Jumlah Atom My XXX Hot Girl
Nukleon, yakni partikel yang terdapat di dalam nukleus/inti atom, terdiri dari neutron dan proton. Jumlah nukleon di dalam suatu atom menentukan massa atom tersebut, yang sering juga disebut nomor nukleon atau nomor massa. Masing-masing nukleon (proton dan neutron) tersusun dari partikel fundamental yang lebih kecil, yakni quark.

Hitunglah jumlah atom C primer, C sekunder, C tersier, da...
Unsur terbagi menjadi tiga jenis, yaitu unsur logam, non logam, dan unsur semi logam. Jumlah atom dari setiap unsur dalam rumus kimia dinyatakan oleh angka indeksnya masing-masing. Amonia terdiri dari unsur N dan H yang merupakan unsur non-logam. Tiap molekul amonia mengandung 1 atom N dan 3 atom H.

Soal Gambarkan rumus struktur lengkap (dengan menunjukkan masingmasing atom dan dengan menggun
Topik 1: Jumlah Atom dalam Rumus Kimia Sub-topik 1: Atom Hidrogen Atom hidrogen merupakan elemen pertama dalam tabel periodik dan memiliki simbol H. Dalam rumus kimia, jumlah atom hidrogen dapat bervariasi tergantung molekul yang terbentuk. Sebagai contoh, dalam air (H 2 O), terdapat 2 atom hidrogen. Sub-topik 2: Atom Oksigen
Rumus Kimia RUANG BACA
Contoh Rumus Empiris. Misalnya n-heksana dengan rumus molekul CH 3 CH 2 CH 2 CH 2 CH 2 CH 3. Senyawa ini mempunyai struktur rantai lurus, 6 atom karbon, dan 14 atom hidrogen. Maka rumus kimia heksana adalah C 6 H 14 , sementara rumus empirisnya yaitu C 3 H7 yang menunjukkan rasio C:H sebanyak 3:7. Hasil analisis pada 6 gram senyawa diperoleh.

Jumlah atom contoh soal kimia SMA YouTube
Nah, rumus molekul ini digolongkan menjadi dua, yaitu rumus molekul unsur dan rumus molekul senyawa. 1. Rumus Molekul Unsur. Rumus molekul unsur adalah rumus yang menyatakan gabungan atom-atom yang sama jenis unsurnya lalu membentuk sebuah molekul. Nah, molekul unsur dibagi lagi menjadi dua berdasar dari jumlah atom yang bergabung.

Lengkapilah tabel berikut! Unsur Nomor Atom Konfigurasi E...
Rumus molekul senyawa merupakan rumus kimia yang menggambarkan jumlah atom dan unsur penyusun suatu senyawa, contoh : C6H12O6 , C4H8, dan lain-lain.. Mr = massa rata-rata 1 molekul senyawa 1/12 massa 1 atom C-12. Contoh Soal 1 Hitunglah Mr CaBr2, bila Ar Ca = 40,078 dan Ar Br = 79,904. Cara Mengenal Karakter Orang Dari 5 Pertanyaan.

hitung jumlah atom dalam molekul (part 1) YouTube
Namun partikel penyusun atom secara mandiri tidak bisa memberikan sifat dasar kimia. Meski terbilang kecil, gaya elektromagnetik atom dapat mengikat partikel-partikel seperti proton, neutron, dan elektron . Dari gambar terlihat bahwa atom berbentuk bola dengan semua proton dan neutron berkumpul di dalam inti atom.

Hitunglah jumlah masingmasing atom penyusun dan rumus kimia berikut, a.3Na No3, b.2cH3 CooH, C
Definisi. Bentuk (rupa) yang lain dari beberapa atom yang memiliki suatu kesamaan pada jumlah partikel dasar penyusunnya, meliputi isotop, isobar, isoton, dan isoelektron. 1. Isotop. Isotop ( isotope ), berasal dari kata dalam bahasa Yunani: isos (artinya: sama) dan topos (tempat) pada dasarnya menyatakan atom-atom yang memiliki tempat yang.

CARA MENENTUKAN JUMLAH PROTON, ELEKTRON, NEUTRON UNSUR Na KIMIA KELAS X SMA YouTube
Pertama-tama, kita hitung massa rata-rata 1 atom unsur klorin terlebih dahulu menggunakan rumus seperti berikut. Lalu, setelah mengetahui massa atom rata-rata dari unsur klorin, selanjutnya kita hitung massa atom relatifnya menggunakan rumus Ar seperti berikut. Jadi, massa atom relatif atau Ar dari klorin tersebut adalah sebesar 0,355.

Hitunglah Jumlah Masing Masing Atom Penyusun Dari Rumus Kimia Berikut JumlahID
Persen massa merupakan persentase masing-masing unsur dalam suatu senyawa kimia.. Carilah bobot atom setiap unsur dalam rumus kimia di tabel periodik. Massa unsur biasanya dapat ditemukan di bawah simbol kimianya.. jumlahkan 2,01588 g/mol (massa dari 2 mol atom hidrogen) dengan 15,9994 g/mol (massa satu mol atom oksigen) menjadi 18,01528.

Hitunglah jumlah atom C primer, sekunder, tersier,...
Jumlah atom pada rumus kimia dituliskan dengan angka di belakang lambang atom,. Tentukan mana yang merupakan rumus molekul dan rumus empiri dari beberapa senyawa berikut ini. a. Li 2 O. d. BaSO 4. g. C 4 H 8 O 2. b. Al 2 O 3. e. CH 3 COOH. h. C 2 H 4. c. C 4 H 10. f. H 2 O 2. i.. Hitunglah jumlah masing-masing atom yang menyusun molekul.

Cara Menghitung Jumlah Atom Dalam Rumus Kimia Gini Caranya Hot My XXX Hot Girl
Hitunglah jumlah masing masing atom penyusun dari rumus kimia berikut a.3Na NO3 - 11540888 anggianggreni anggianggreni 09.08.2017 Kimia Sekolah Menengah Pertama terjawab • terverifikasi oleh ahli hitunglah jumlah masing masing atom penyusun dari rumus kimia berikut a.3Na NO3 2

Jumlah atom contoh soal kimia YouTube
Jumlah mol dapat dihitung menggunakan rumus berikut: n = PV/RT. [2] Di dalam rumus ini, n adalah jumlah mol, P adalah tekanan, V adalah volume, T adalah suhu dalam Kelvin, dan R adalah konstanta gas. Contoh: n = PV/RT = (0,984 atm * 1 L) / (0,08206 L atm mol-1 K-1 * 318,15 K) = 0,0377 mol 3 Hitunglah berat molekul gas.