
Cara Menentukan Bilangan Oksidasi yang Mudah, Berikut Penjelasannya
Tetapkan bilangan oksidasi -2 pada oksigen (tanpa perkecualian). Dalam hampir semua kasus, atom oksigen memiliki bilangan oksidasi -2. Ada beberapa perkecualian dalam peraturan ini: Saat oksigen berada dalam bentuk unsur (O 2 ), bilangan oksidasinya adalah 0, karena ini adalah peraturan untuk semua atom unsur.

Peristiwa Pelepasan Oksigen Disebut Dengan….
Ion monoatomik adalah ion yang hanya terdiri dari satu atom. Bilangan oksidasinya sama dengan muatannya. Contoh: Bilangan oksidasi pada Li+, Na+, K+,dan Ag+ adalah +1.. Bilangan Oksidasi Oksigen dalam Senyawanya Adalah -2. Bilangan oksidasi oksigen dalam senyawanya adalah -2, kecuali dalam senyawa peroksida dan OF2. Contoh: Bilangan oksidasi.
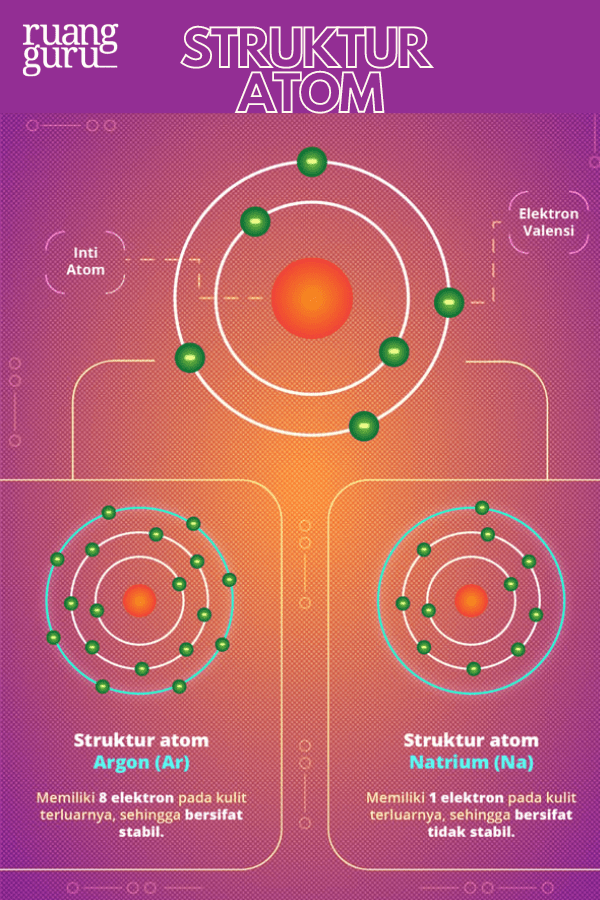
Cara Menentukan Bilangan Oksidasi dan Contohnya
S O 2 SO_2 Tentukan bilangan oksidasi sulfur S S dan oksigen O O . Bilangan oksidasi sulfur adalah +4, dan oksigen -2. Nama senyawa ini menjadi "sulfur dioxide." Contoh Soal Redoks. Tentukan apakah reaksi berikut merupakan reaksi oksidasi, reduksi, atau reaksi redoks. Tuliskan bilangan oksidasi dari setiap unsur yang.

Elektron Valensi Oksigen Studyhelp
Bilangan oksidasi atom F yaitu -1. Atom logam selalu mempunyai bilangan oksidasi positif dengan harga yang sesuai pada nomor golongannya, kecuali dengan logam transisi yang mempunyai biloks lebih dari satu. - Bilangan oksidasi Li, Na, K, Rb, dan Cs yaitu +1. - Bilangan oksidasi Be, Mg, Ca, Sr, Ba, dan Ra yaitu +2. - Bilangan oksidasi Al yaitu +3.

Pada reaksi 2CO+2NO > 2CO2+N2 Bilangan oksidasi C beru...
- Oksidator adalah sumber oksigen pada reaksi oksidasi atau zat yang mengalami reduksi. c. Penjelasan. 2. Bilangan oksidasi ion monoatom (1 atom) dan poliatom (lebih dari 1 atom) sesuai dengan jenis muatan ionnya. Contohnya adalah sebagai berikut. a. Bilangan oksidasi ion monoatom Na+, Mg2+, dan Al3+ berturut-turut adalah +1, +2, dan +3.

Perhatikan pernyataan berikut (1)Bilangan oksidasi O pada molekul O2 adalah 0 (2)Bilangan
Aturan Penentuan Bilangan Oksidasi. Setelah memahami pengertian, Sobat Zenius juga harus tahu aturan biloks. Aturan yang menentukan bilangan oksidasi yang benar adalah: Unsur Bebas → Biloks = 0. Contoh: Na, K, Cl 2, M 2, dan O 2. Logam yang Berikatan dengan Unsur Lain → Biloks = Positif. Contoh: Gol I: Na, K, Rb → biloks = +1

Contoh Soal Reduksi Oksidasi
1. Berdasarkan penangkapan atau pelepasan oksigen. Oksidasi: reaksi yang melibatkan penangkapan atom oksigen. Contoh: C+ O2 → CO2. Atom C (karbon) mengalami oksidasi karena dalam reaksi atom karbon mengikat atom oksigen menjadi CO2. Reduksi: reaksi yang melibatkan pelepasan atom oksigen. Contoh: H2O2 → H2O + O2.

Bilangan Oksidasi Atom Mn YouTube
Aturan menentukan bilangan oksidasi dijabarkan pada poin-poin di bawah ini: Bilangan oksidasi atom F yaitu -1. Atom logam selalu mempunyai bilangan oksidasi positif dengan harga yang sesuai pada nomor golongannya, kecuali dengan logam transisi yang mempunyai biloks lebih dari satu. - Bilangan oksidasi Li, Na, K, Rb, dan Cs yaitu +1.
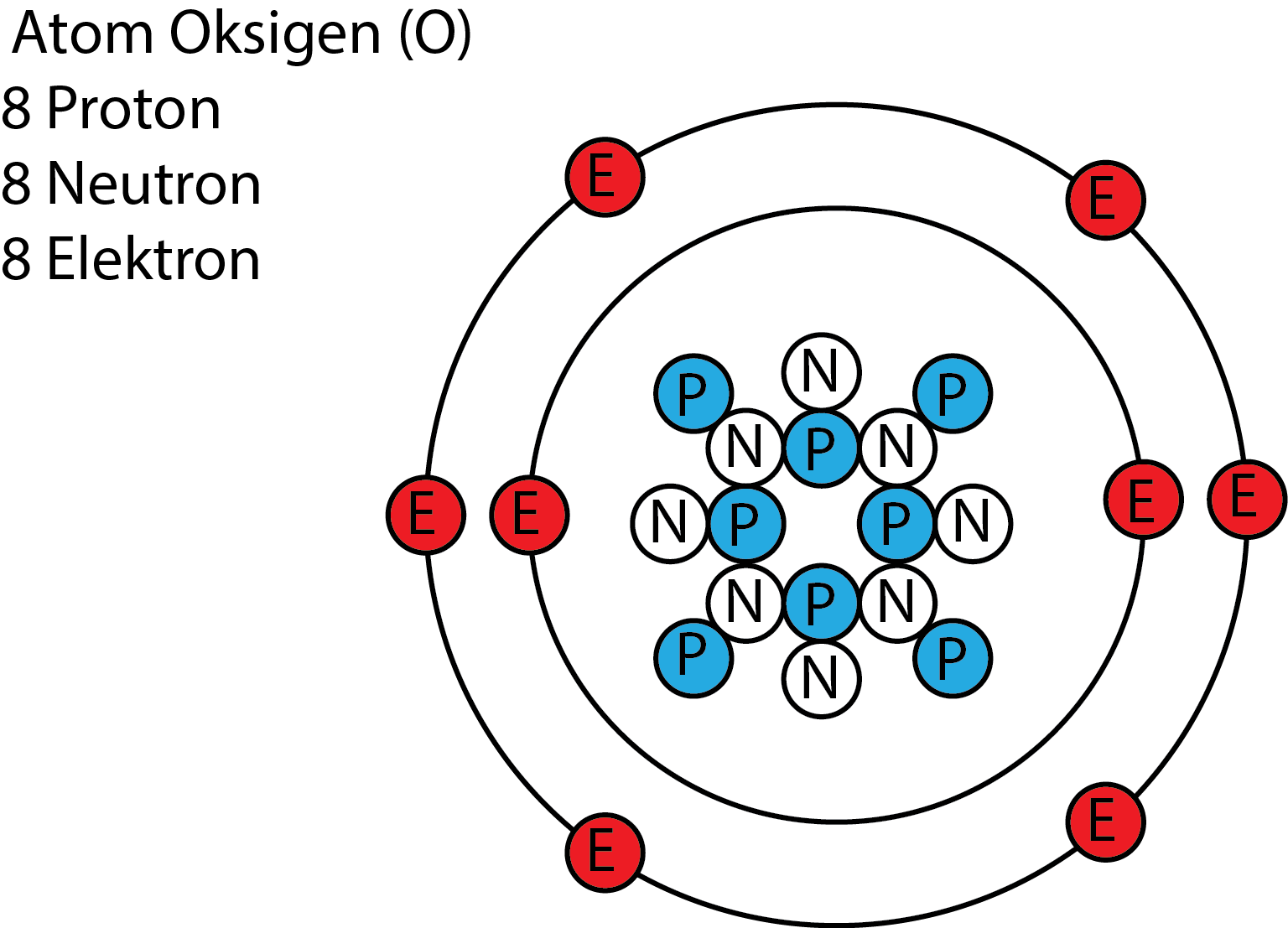
Molekul Unsur dan Senyawa Kimia Kenal Sains
Sifat atom; Bilangan oksidasi: −2, −1, 0, +1, +2: Elektronegativitas: Skala Pauling: 3,44 :. Keadaan oksidasi oksigen adalah -2 untuk hampir semua senyawa oksigen yang diketahui. Keadaan oksidasi -1 ditemukan pada beberapa senyawa seperti peroksida. Senyawa oksigen dengan keadaan oksidasi lainnya sangat jarang ditemukan, yakni -1/2.

Representasi Geometri Struktur Atom Oksigen YouTube
Bilangan oksidasi unsur S pada Na 2 S dan MgS adalah -2. Bilangan oksidasi unsur Cl pada NaCl, KCl, MgCl 2, dan FeCl 3 adalah -1. 5. Bilangan oksidasi unsur H pada senyawanya adalah +1.' Kecuali dalam hidrida (senyawa hydrogen dengan logam), bilangan oksidasinya -1′ Alasan: dalam senyawa hidrida, hidrogen ada dalam bentuk ion hidrida, H.

Struktur Atom Oksigen MateriKimia
Unsur bebas dengan bentuk atom, sebagai contoh: Cu, K, Ca, C, Nae, Fe, Al, Na;. Jadi terbukti jika bilangan oksidasi H bertemu logam (Al) adalah -1. 8. Bilangan Oksidasi Oksigen (O) adalah -1 dalam Senyawa Peroksida dan -2 dalam Senyama Non-Peroksida. Contoh dari penerapan aturan ini seperti misalnya pada H 2 O 2 (hidrogen peroksida.

Cara Menentukan Bilangan Oksidasi S dalam Ion S2O82 dan S4O62 yang Benar YouTube
Sekali lagi, ini adalah nilai rata-rata karena struktur molekulnya adalah H 3 C−CH 2 −CH 3, dengan atom karbon pertama dan ketiga masing-masing memiliki bilangan oksidasi −3 dan atom pusat −2. Contoh dengan bilangan oksidasi pecahan yang benar untuk atom yang setara adalah kalium superoksida, KO 2.
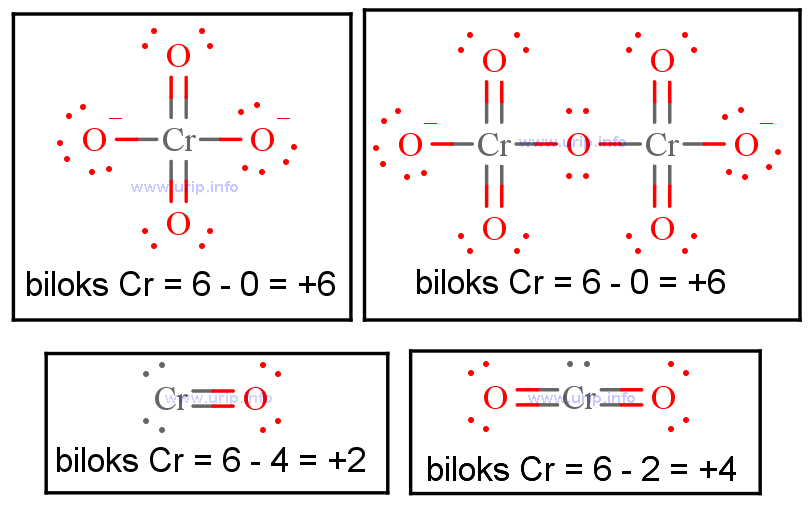
Catatan tentang Bilangan Oksidasi Serba Ada
Oke, kita lanjut ya bahasannya! Pada reaksi redoks, terdapat unsur-unsur yang bertindak sebagai reduktor dan oksidator. Zat yang mengalami oksidasi itu disebut reduktor, sedangkan zat yang mengalami reduksi disebut oksidator. Coba perhatikan contoh berikut ini, ya! Reaksi: Mg(s) + 2HCl -----> MgCl2(aq) + H2(g) Karena Mg merupakan unsur bebas, jadi biloks Mg = 0.

Contoh Reaksi Reduksi Dan Oksidasi Berdasarkan Perubahan Bilangan Oksidasi Sketsa
Zn (s) + Cu2+(aq) → Zn2+(aq) + Cu (s) Reaksi keseluruhan adalah jumlah dari kedua setengah reaksi, yaitu setengah reaksi oksidasi dan setengah reaksi reduksi yang disebut reaksi redoks. Reaksi di atas menunjukkan terjadinya pelepasan dan pengikatan elektron, maka dapat disimpulkan sebagai berikut. Oksidasi adalah peristiwa pelepasan elektron.

Jumlah atom oksigen dalam senyawa kapur Ca(OH)2 adalah
Ada 8 aturan dalam menentukan bilangan oksidasi suatu unsur, di antaranya: 1. Bilangan oksidasi unsur bebas adalah 0. Unsur bebas adalah unsur yang tidak bergabung atau berikatan secara kimia dengan unsur lain. Unsur bebas terbagi menjadi dua, yaitu unsur bebas berbentuk atom, seperti C, Ca, Cu, Na, Fe, Al, Ne dan unsur bebas berbentuk molekul.

Nilai Bilangan Oksidasi Dari S Didalam Na2so 3 Adalah peristiwa yang terjadi pada fabel
Bedakan dengan bilangan oksidasi. Dalam kimia, keadaan oksidasi merupakan indikator derajat oksidasi sebuah atom dalam suatu senyawa kimia.Keadaan oksidasi formal merupakan muatan hipotetis yang suatu atom peroleh apabila semua ikatan yang berikatan dengan atom tersebut adalah sepenuhnya bersifat ionik.Keadaan oksidasi berupa bilangan bulat, ia dapat berupa nilai positif, negatif, ataupun nol.