
Titrasi AsamBasa
Ekuivalen secara kimia ini artinya jumlah titran yang bereaksi adalah sesuai secara stoikiometri dengan yang dibutuhkan oleh analit. Untuk lebih mudah memahami ini maka saya akan contohnya dari reaksi berikut ini. Titik ekuivalen pada saat kita menitrasi larutan NaCl dengan AgNO3 dicapai saat 1 mol AgNO3 tepat bereaksi dengan 1 mol NaCl.

Titrasi dihentikan apabila sudah tercapai titik akhir tit...
Dengan persamaan ini, kita dapat menetapkan hubungan stoikiometri antara jumlah mol asam dan basa yang bereaksi selama titrasi. Hal ini membantu dalam perhitungan konsentrasi larutan yang diukur. Penting untuk memilih indikator pH yang tepat yang akan berubah warna di sekitar titik ekivalen untuk mempermudah penentuan titik akhir titrasi.

Titrasi Asam basa_Kadar Asam asetat (Tutorial Prosedur + Perhitungan) YouTube
3. Titik Akhir (TA) Titik Akhir (TA) : pH pada saat indikator berubah warna. Cara atau metode titrasi: Larutan yang akan diteteskan dimasukkan ke dalam buret (pipa panjang berskala), inilah yang disebut peniter; Larutan yang akan dititrasi dimasukkan ke dalam erlenmeyer dengan mengukur volumenya terlebih dahulu memakai pipet volume

Titrasi Argentometri Titrasi Pengujian Kadar Klorida (Sampel Air Sungai) YouTube
Titik ekuivalen adalah titik yang mennjukkan saat titran yang ditambahkan bereaksi seluruhnya dengan zat tang dititrasi. Dengan kata lain, pada titik ekuivalen jumlah mol titran setara dengan jumlah mol titrat menurut stoikiometri. Perlu kita ketahui bahwa titik ekuivalen bukanlah titik akhir. Titik atau keadaaan dimana reaksi telah berjalan.
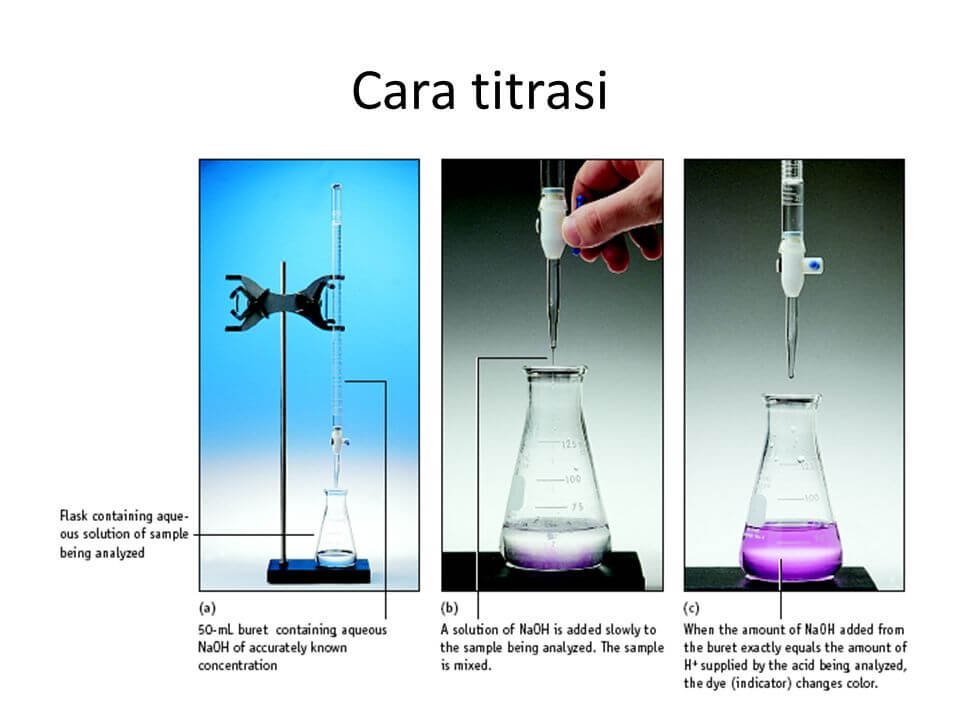
Prinsip Kerja Titrasi Panduan Lengkap dan Komprehensif
Dalam titrasi asam basa terdapat dua istilah penting yang harus dipahami yaitu titik ekuivalen dan titik akhir titrasi. Perbedaan kedua istilah tersebut dapat dijelaskan sebagai berikut. Titik ekuivalen (TE) adalah titik saat asam basa tepat habis bereaksi (secara teoritis). Titik akhir (TA) titrasi adalah titik saat indikator asam basa.

Percobaan titrasi antara 10 mL larutan H2SO4 dengan NaOH
Larutan yang belum diketahui konsentrasinya ditambahkan beberapa tetes indikator, setelah itu ditetesi dengan larutan yang sudah diketahui konsentrasinya. Titik akhir titrasi ialah tepat pada saat terjadi sebuah perubahan warna indikator. Titrasi yang melibatkan reaksi asam serta basa disebut dengan titrasi asam-basa.
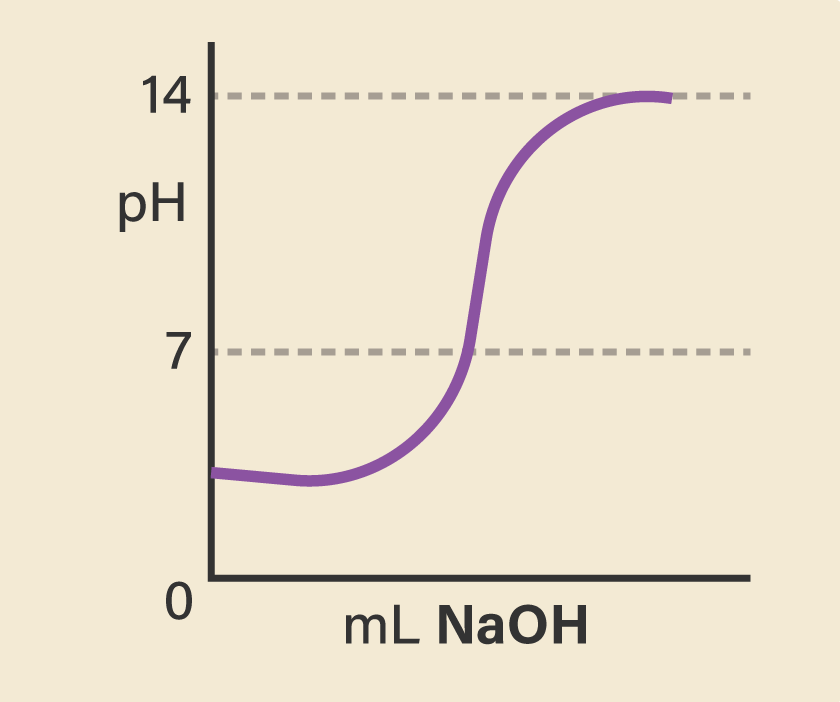
Kurva yang menunjukkan hasil titrasi HCl dan NaOH
Pada titrasi ini digunakan indikator fenolftalein (PP) dengan trayek pH 8.3-10 dimana titik akhir titrasi atau ditunjukkan ketika warna larutan berubah menjadi merah muda. Hal ini menunjukkan bahwa basa yang digunakan telah berlebih sehingga bereaksi dengan PP menghasilkan warna merah muda.

Perhatikan gambar titrasi berikut! Sebanyak
Setelah proses titrasi selesai, yang ditandai dengan perubahan warna pada larutan sampel, untuk membaca hasil titrasi asam basa adalah dengan melihat skala volume permukaan cairannya. Misalnya, permukaan cairan pada buret setelah titrasi, berada pada skala 20 ml. Maka, volume standar atau titran yang terpakai sebesar 20 ml.

Jenis dan Metode Titrasi, Cara Melakukan yang Baik dan Benar, Praktikum, Menentukan Titik Awal
Pengertian Titik Ekuivalen Titrasi, 5 Cara Menentukan, dan Contohnya. Oleh Aji PangestuDiposting pada 2 Maret 20222 Maret 2022. Keakuratan hasil dari sebuah titrasi akan sangat bergantung pada penentuan titik ekuivalen serta penentuan titik akhir titrasi. Maka dari itu, setidaknya seorang analis yang melakukan harus teliti dan menguasai betul.
Video belajar Titik Ekuivalen dan Titik Akhir Titrasi Kimia untuk Kelas 12
suatu titrasi, segala sesuatu yang berkaitan dengan titik ekivalen dan titik akhir titrasi, pengamatan, perhitungan dan pengolahan data volume serta kurva titrasi menjadi sangat penting untuk diperhatikan. Contoh analisis yang menggunakan teknik titrasi adalah penentuan konsentrasi larutan Asam klorida melalui titrasi dengan larutan natrium.

Seorang siswa melakukan percobaan titrasi untuk menghitun...
Titik akhir titrasi adalah kondisi pada saat terjadi perubahan warna dari indikator. Titik akhir titrasi diharapkan mendekati titik ekivalen, yaitu kondisi pada saat larutan asam tepat bereaksi dengan larutan basa. Pemilihan indikator disesuaikan dengan titik ekuivalen teoritis, dimana indikator yang digunakan harus mencakup / mendekati titik.

Titrasi Asam Basa Pengertian Cara Kerja Jenis Rumus Dan Contoh Soal Dengan Penjelasan Riset
Penambahan larutan penitrasi ke dalam erlenmeyer dihentikan ketika sudah terjadi perubahan warna dalam erlenmeyer. Perubahan warna ini menandakan telah tercapainya titik akhir titrasi (titik ekuivalen). Langkah 5: Mencatat volume yang dibutuhkan larutan penitrasi dengan melihat volume yang berkurang pada buret setelah dilakukan proses titrasi.

Titik akhir titrasi adalah
Kesalahan titrasi kompleksometri tergantung pada cara yang dipakai untuk mengetahui titik akhir. Pada prinsipnya ada dua cara, yaitu kelebihan titran yang pertama ditunjukkam atau berkurangnya konsentrasi komponen tertentu sampai 153 batas yang ditentukan, dideteksi. Pertama, kesalahan titrasi dihitung dengan cara yang sama pada titrasi.

Apa Yang Dimaksud Dengan Titrasi Iodometri Dan Titrasi Iodimetri My XXX Hot Girl
Indikator ini digunakan untuk memudahkan penentuan titik akhir titrasi dengan memberikan sinyal visual saat titik akhir titrasi tercapai. Berikut adalah beberapa jenis indikator yang digunakan dalam titrasi: Fenolftalein - indikator ini digunakan untuk menentukan titik akhir titrasi yang bersifat asam-basa. Secara umum, fenolftalein berubah.

Apa yang Dimaksud dengan Titran?
Titrasi fase gas adalah titrasi yang dilakukan dalam fase gas, khususnya sebagai metode untuk menentukan spesies reaktif melalui reaksi dengan kelebihan beberapa gas, yang bertindak sebagai titran. Dalam satu titrasi fase gas yang umum, gas ozon dititrasi dengan nitrogen oksida sesuai reaksi berikut. O 3 + NO → O 2 + NO 2.
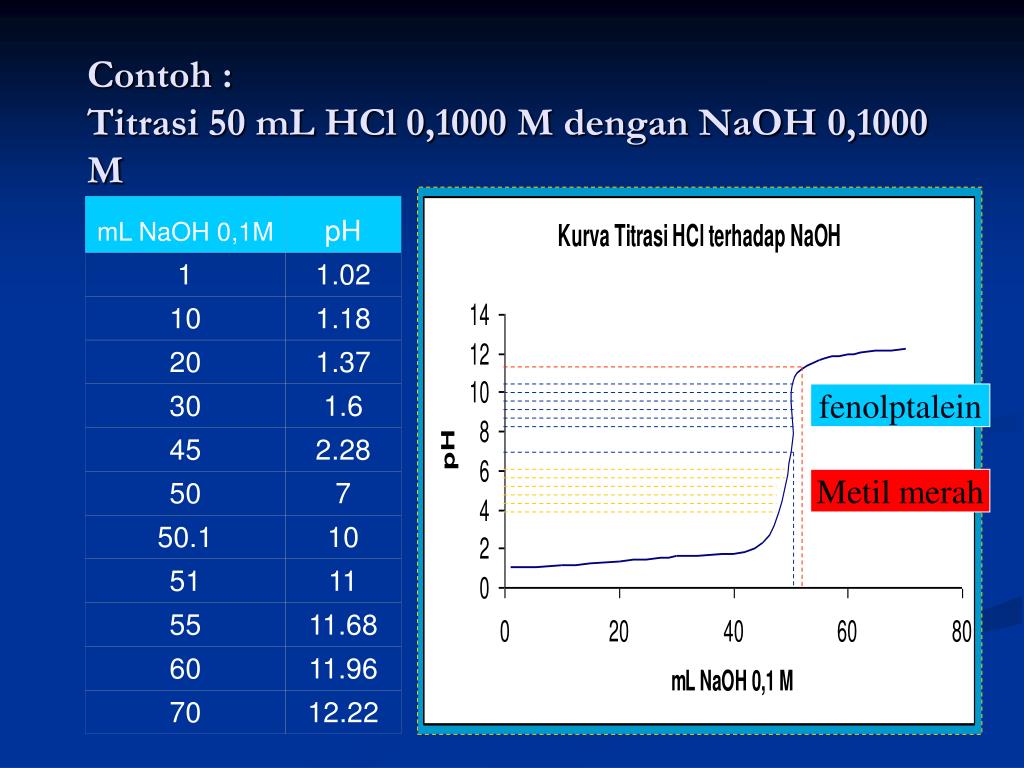
PPT Kurva Titrasi PowerPoint Presentation, free download ID4805744
Prinsip dasar dari titrasi adalah mencapai titik ekivalen atau titik akhir, di mana jumlah mol zat dalam larutan titran berada dalam stoikiometri yang tepat dengan zat yang sedang dianalisis dalam larutan analit. Proses titrasi ini bergantung pada beberapa faktor untuk mencapai titik akhir titrasi yang setimbang. Berikut ini beberapa faktor.